Rất nhiều người đang thắc mắc benzen là gì? Công thức cấu tạo của benzen như thế nào? Tính chất vật lý và hóa học của benzen? Bài tập về benzen? Để lý giải tất cả những thắc mắc này, mời bạn đọc cùng đón xem bài viết bên dưới nhé.
Xem thêm:
- Khí CO2 là gì? Công thức cấu tạo đúng của CO2 là gì?
- Khái niệm, công thức cấu tạo của Etilen đầy đủ và bài tập về Etilen
Định nghĩa của Benzen là gì?
Benzen là một hydrocacbon thơm, tan ít trong nước nhưng lại là một chất hòa tan dễ dàng trong dầu khoáng, dầu động vật thực vật, dung môi hữu cơ… Đặc biệt là mỡ, sơn, vecni, cao su, nhựa đường…
Benzen là thành phần tự nhiên của dầu mỏ, một trong những hóa chất dầu cơ bản nhất. Bởi những liên kết pi liên tục tuần hoàn giữa những nguyên tử cacbon, benzen được phân loại là hydrocacbon thơm.
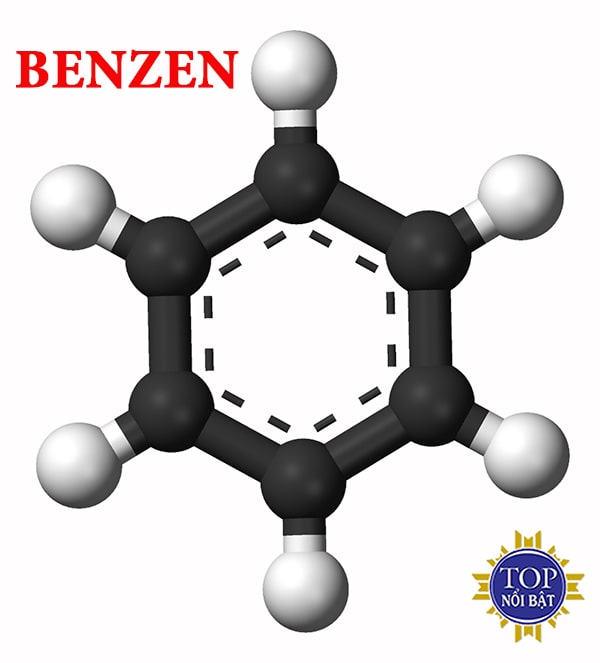
Công thức cấu tạo của Benzen chuẩn nhất
- Công thức hóa học của Benzen là C6H6
- Công thức cấu tạo của benzen là:
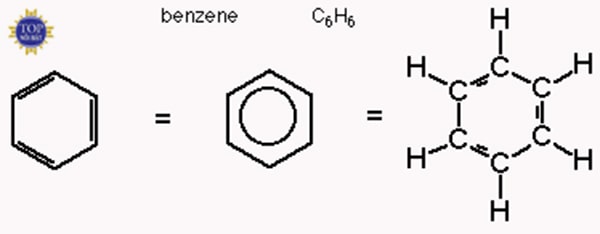
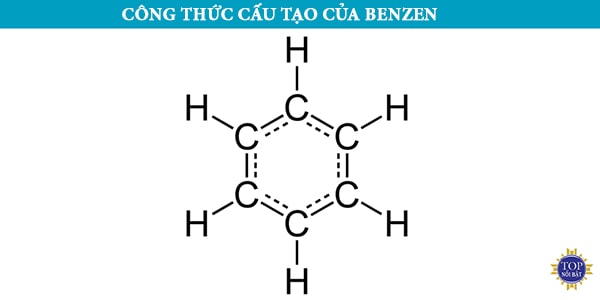
Từ công thức cấu tạo của benzen ở trên có thể thấy 6 nguyên tử cacbon liên kết với nhau để tạo nên vòng sâu cạnh đều, có 3 liên kết đôi xen kẽ ba liên kết đơn.
Tính chất hóa học và vật lý của Benzen
Tính chất vật lý của Benzen
- Benzen là chất lỏng vô cùng linh động, không có màu, cò mùi đặc trưng và có nhiệt độ sôi là 800C.
- Benzen nhẹ hơn nước, không tan trong nước, nhưng tan nhiều trong những dung môi hữu cơ như rượu, chất béo, cao su, ete…
- Những đồng đẳng cơ bản của benzen thường tồn tại dưới dạng chất lỏng còn những đồng đẳng cao hơn thì sẽ tồn tại dưới dạng chất rắn.
Tính chất hóa học của Benzen
- Tác dụng với oxi
Khi mà đốt cháy benzen trong không khí tạo ra CO2 và H2O, thì ngọn lửa có nhiều khói đen do trong không khí không cung cấp đủ oxi để có thể đốt cháy hoàn toàn C6H6.
C6H6 + 15/2 O2 → 6CO2 + 3H2O
- Phản ứng thế với Brom
Benzen không làm mất màu dung dịch brom giống như etilen và axetilen. Mà nó chỉ tham gia phản ứng thế với brom lỏng và cần có xúc tác là bột sắt.
C6H6 + Br2 → HBr + C6H5Br (brom benzen)
Ngoài ra, benzen chỉ phản ứng với brom nguyên chất không phản ứng với dung dịch nước brom hay benzen không làm mất màu dung dịch brom khi ở điều kiện bình thường.
- Phản ứng cộng với H2 và Cl2
Benzen khó có thể tham gia phản ứng cộng hơn etilen và axetilen. Nhưng trong điều kiện thích hợp thì benzen C6H6 có phản ứng cộng với một số chất như H2 hay Cl2…
C6H6 + H2 → C6H12
C6H6 + Cl2 → C6H6Cl2 (Hexacloxidohexan)
C6H6Cl6: Hexacloxiclohexan là loại thuốc trừ sâu 6,6,6
Do phân tử có cấu tạo đặc biệt nên benzen vừa có phản ứng thế mà lại có phản ứng cộng.
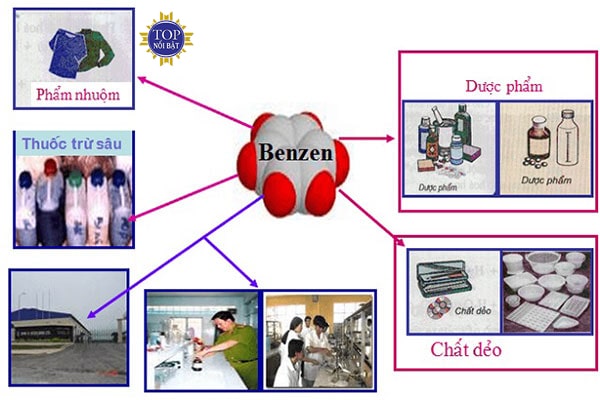
Những ứng dụng của Benzen trong đời sống
- Benzen được ứng dụng trong ngành công nghiệp, sử dụng phổ biến công nghiệp hóa hữu cơ. Đặc biệt, chúng được sử dụng để tổng hợp những monome trong sản xuất polime làm chất dẻo, cao su, tơ sợi.
- Nó được sử dụng để làm dung môi hòa tan như mỡ, cao su, vecni
- Dùng để tẩy mỡ ở xương, da sợi, vải, len, dạ, lau khô, tẩy mỡ trên những tấm kim loại.
- Dùng để điều chế những chất như nitrobenzen, anlin, phenol, tổng hợp phẩm nhuộm, dược phẩm, thuốc trừ hại cho da, cumen, axetan và phenol.
Cách điều chế Benzen tốt nhất
- Điều chế từ axetilen
Phản ứng trùng hợp axetilen xảy ra khi mà có chất xúc tác là C, đun nóng nó ở nhiệt độ là 6000C.
3CH = CH → C6H6
- Điều chế từ axit benzoic
C6H5COOH + NaOH → C6H6 + Na2CO3
- Điều chế từ chưng cất nhựa than đá
- Điều chế từ xiclohexan dùng chất xúc tác là Pt và đun nóng
C6H12 → C6H6 + 3H2
- Điều chế từ n – hexan có xúc tác và đun nóng
C6H14 → C6H6 + 4H2
Một số bài tập về Benzen có lời giải chi tiết
Bài tập 1: Cho benzen tác dụng với lượng dư HNO3 đặc có xúc tác với H2SO4 đặc để điều chế nitrobenzen. Khối lượng nitrobenzen điều chế được từ 18,5 tấn benzen (với hiệu suất phản ứng là 70%) là bao nhiêu tấn?
Lời giải
Ta có:
C6H6 + HONO2 → C6H5NO2 + H2O
m = (18,5/78).123.(70/100) = (tấn)
Bài tập 2: Hỗn hợp khí X gồm 0,1 mol C2H2; 0,2 mol C2H4 và 0,3 mol H2. Khi đun nóng X với xúc tác Ni, sau một thời gian sẽ thu được hỗn hợp khí Y có tỉ khối so với H2 là 10. Hỗn hợp Y phản ứng tối đa với a mol Br2 trong dung dịch. Hỏi giá trị của a là bao nhiêu?
Lời giải
my = mx = 0,1 x 26 + 0,2 x 28 + 0,3 x 2 = 8,8 (g)
=> my = 10 x 2 = 20 => ny = 0,4 mol
Số mol H2 tham gia phản ứng là nx – ny = (0,1 + 0,2 + 0,3) – 0,4 = 0,2 mol
NH2(pư) + nBr2 = 2nC2H2 + nC2H4 => nBr2 = 2 x 0,1 + 0,2 – 0,2 = 0,2 mol
Hy vọng với những kiến thức về benzen ở trên sẽ giúp bạn hiểu về định nghĩa, công thức cấu tạo, điều chế và ứng dụng của benzen. Nếu bạn đọc còn gặp khó khăn trong khi giải bài tập thì hãy để lại bình luận bên dưới nhé.







