Cái tên Etilen không còn xa lạ đối với những bạn học chuyên Hóa Học, nhưng đối với những bạn không chuyên khi làm bài tập về etilen thì lại mông lung, rất mơ hồ về công thức cấu tạo của etilen. Chính vì thế, bài viết hôm nay Top Nổi Bật sẽ giúp bạn đọc hiểu toàn bộ khái niệm, công thức, tính chất vật lý và hóa học, ứng dụng của etilen và cho một số bài tập về etilen có lời giải chi tiết để bạn đọc dễ hiểu nhất.
Xem thêm:
- Công thức cấu tạo của Metan và bài tập về Metan có lời giải
- Khí CO2 là gì? Công thức cấu tạo đúng của CO2 là gì?
- Công thức cấu tạo của Benzen CHUẨN NHẤT và bài tập minh họa
Định nghĩa về Etilen
Etilen hay còn có tên gọi khác là Ethylene chính là một chất khí, một trong những loại hidrocacbon, và cũng là một anken đơn giản nhất.
Etilen được biết đến là một trong những chất khí sinh học đầu tiên mà con người biết đến, đây là loại khí Olefin đơn giản. Bởi vậy mà Etilen rất quen thuộc đối với mỗi chúng ta, hay trong chính mỗi gia đình Việt.
Công thức cấu tạo của Etilen đầy đủ
Công thức cấu tạo Etilen là C2H4. Được viết ngắn gọn là CH2 = CH2
Ngoài ra, phân tử khối của Etilen là 28 và cấu tạo phân tử như sau:
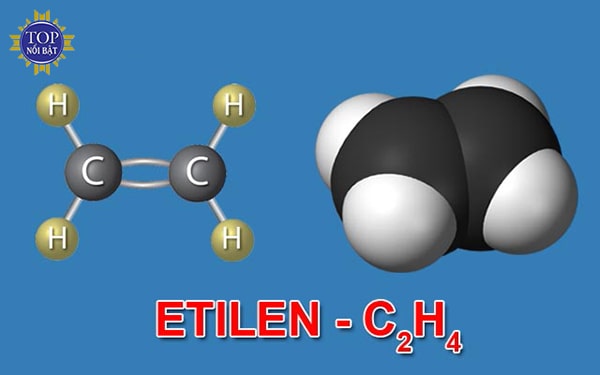
Chú ý: Trong phân tử C2H4 có một liên kết đôi giữa hai nguyên tử cacbon. Trong liên kết đôi có một liên kết kém bền dễ đứt trong những phản ứng hóa học. Những hidrocacbon mạch hở, trong phân tử có một liên kết đôi như etilen gọi là anken có công thức chung là CnH2n (với n ≥ 2).
Tính chất hóa học và tính chất vật lý của Etilen
Tính chất hóa học Etilen
Etilen tác dụng được với nhiều chất ở nhiều dạng khác nhau như khí oxy, dung dịch brom, phản ứng trùng hợp của etilen… Etilen là một chất khí hoàn toàn không thể trơ về Hóa Học, nó có thể tham gia phản ứng ở nhiều dạng khác nhau, cụ thể như sau:
- Khi tác dụng với oxi: Khi đốt cháy oxi, atilen cháy sẽ tạo thành khí CO2 và H2O và tỏa ra nhiều nhiệt. PTHH:
C2H4 + 3O2 → 2CO2 + 2H2O + Q
- Khi etilen tác dụng với brom ở dạng dung dịch. PTHH:
CH2 = CH2 + Br2 → Br – CH2 – CH2 – Br
- Với đặc điểm những chất liên kết đôi dễ tham gia phản ứng cộng. Phân tử etilen kết hợp vưới nhau (còn có tên gọi khác là phản ứng trùng hợp). Những phân tử etilen kết hợp với nhau sẽ tạo thành chất có phân tử lượng rất lớn được gọi là PolyEtilen hay PE. PTHH:
…+ CH2 = CH2 + CH2 = CH2 + … → … CH2 – CH2 – CH2 – CH2 – …
Tính chất vật lý của Etilen
Etilen là chất khí không có màu, không có mùi, nhẹ hơn không khí, ít tan trong nước, dễ bắt cháy và đặc biệt là có mùi ngọt nhẹ của xạ hương.
Ứng dụng của Etilen trong đời sống hàng ngày
Ứng dụng trong công nghiệp
- Sử dụng trong sản xuất bao bì
- Nguyên vật liệu trong xây dựng
- Dùng trong ngành dệt may, điện tử.
- Sử dụng trong ngành hóa dầu, chất dẫn xuất
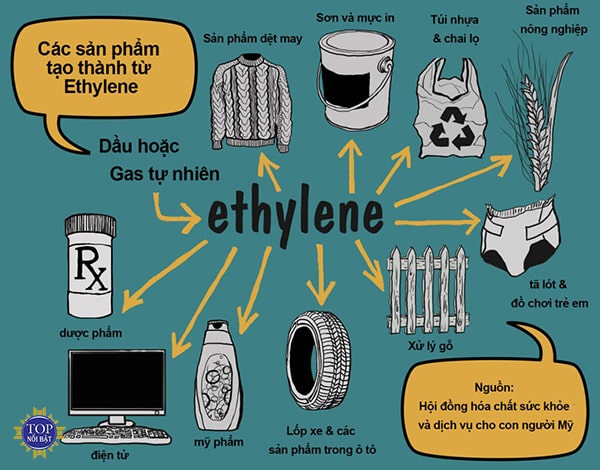
Ứng dụng trong nông nghiệp
- Kích thích sự tăng trưởng của những tế bào thực vật
- Kích thích nảy mầm hay quá trình sinh trưởng của nhiều loại cây trồng
- Kích thích các loại quả mau chín, để tăng nâng suất cây trồng.
Ứng dụng trong sinh học
- Kích thích các loại quả nhanh chín
- Ức chế sự rơi rụng của hoa, quả, cành, lá
Những bài tập về Etilen có lời giải dễ hiểu
Bài tập 1: Để đốt cháy 5,58 lít khí etilen cần phải sử dụng:
a. bao nhiêu lít oxi?
b. bao nhiêu lít khí chứa 20% thể tích khí oxi? Biết thể tích những khí đo ở điều kiện tiêu chuẩn.
Lời giải
a. PT phản ứng cháy etilen là:
C2H4 + 3O2 → 2CO2 + 2H2O
NC2H4 = 5,58/22,4 = 0,25 mol
Theo PT nO2 = 3.nC2H4 = 0,25 x 3 = 0,75 mol
VO2 = 0,75 x 22,4 = 16,8 lít
b. Thể tích không khí = (16,8.100)/20 = 84 lít
Bài tập 2: Dẫn 6,6 lít hỗn hợp khí ở điều kiện tiêu chuẩn bao gồm metan và etilen qua bình đựng lượng dư brom thấy khối lượng bình tăng 2,9 gam. Hỏi thể tích khí metan (đktc) trong hỗn hợp là bao nhiêu?
Lời giải
Khối lượng bình brom tăng chính là khối lượng etilen phản ứng như sau:
netilen = 2,9/29 = 0,1 mol
Vetilen = 0,1.22,4 = 2,24 lít
Vmetan = 6,6 – 2,24 = 4,36 lít
Bài tập 3: Dẫn 3,8 lít hỗn hợp gồm metan và etilen (đktc) qua lượng dư dung dịch brom thấy thu được 5,7 gam dibrometan. Phần trăm thể tích khí metan trong hỗn hợp ban đầu là bao nhiêu?
Lời giải
Dẫn metan và etilen qua dung dịch brom, chỉ có etilen phản ứng như sau:
C2H4 + Br2 → C2H4Br2
0,025 0,025 mol
%VCH4 = 100% – [(0,025.22,4)/3,8].100% = 85%
Hy vọng rằng bài viết trên đây của chúng tôi sẽ giúp bạn hiểu toàn bộ kiến thức về etilen, nhớ công thức và biết áp dụng công thức vào bài tập một cách phù hợp nhất. Nếu như bạn vẫn còn khó khăn trong khi giải bài tập hay còn thắc mắc nào chưa được giải đáp thì hãy để lại bình luận bên dưới nhé, chúng tôi sẽ giúp bạn giải đáp thắc mắc đó nhanh nhất.







