Trong môn hóa học, nồng độ PH- là kiến thức vô cùng quan trọng mà học sinh cần phải nắm vững để có thể giải được những bài tập liên quan. Vậy PH là gì? Công thức tính nồng độ PH như thế nào? Bài tập tính nồng độ PH? Hãy cùng Top Nổi Bật tìm hiểu chi tiết trong bài viết sau đây nhé.
Xem thêm:
- [Tổng Hợp] công thức tính phần trăm trong Excel đơn giản, dễ làm
- Công thức tính bình quân gia quyền kèm ví dụ minh họa
- Công thức tính độ che phủ rừng đầy đủ kèm ví dụ minh họa
PH là gì?
PH được hiểu là chỉ số đo hoạt động của những ion Hydro (H+) trong dung dịch. Nếu như lượng ion H+ trong dung dịch nhiều, hoạt động mạnh thì dung dịch đó mang tính axit và ngược lại nếu lượng ion H+ thấp thì dung dịch đó có tính bazo. Trong trường hợp lượng hydro (H+) cân bằng với lượng hydroxit (OH-) thì tức là dung dịch đó trung tính, độ PH khi đó xấp xỉ bằng 7.
Độ PH chính là chỉ số để xác định tính axit hay bazo của nước hay một loại dung dịch nào đó.
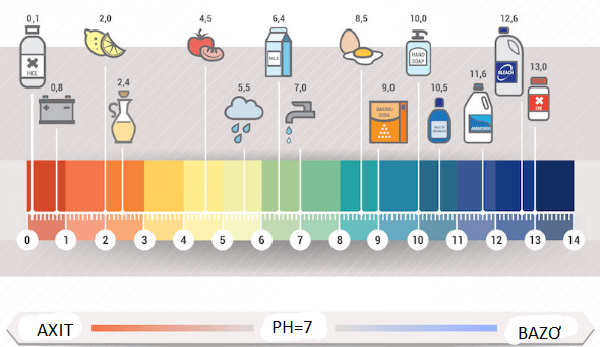
Công thức tính nồng độ PH-
Công thức chung để tính pH của dung dịch là:
PH = -log.[H+]
Trong đó có [H+] là chỉ số hoạt động của ion H+
Ngoài việc áp dụng công thức chung ở trên thì ta còn có công thức tính nồng độ pH của axit và bazo chuyển đổi khác là:
PH = 14 – pOH (Với pOH = -log[OH-] = log(1/[OH-])
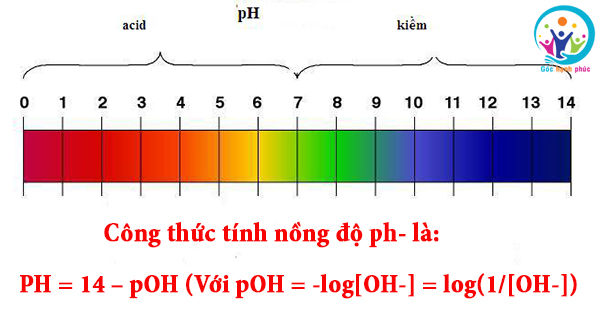
Bài tập tính nồng độ PH có lời giải dễ hiểu
Bài tập 1: Trộn 20g dung dịch HCl 8,3% với 25g dung dịch H2SO4 5,9% rồi thêm nước để được 100ml dung dịch A. Tính PH của dung dịch A bằng bao nhiêu?
Lời giải
Số mol HCl là nHCl = (20.8,3)/(100.36,5) = 0,04 mol
Số mol H2SO4 là nH2SO4 = (25.5,9)/(100.98) = 0,01 mol
Phương trình điện ly:
HCl → H+ + Cl
0,04 → 0,04 mol
H2SO4 → 2H+ + SO42-
0,01 → 0,04 mol
Tổng số mol H+ là nH+ = 0,04 + 0,04 = 0,08 mol
CM(H+) = 0,08/0,1 = 0,8 M => PH = 0,8
Bài tập 2: Hòa tan 4,66 gam hỗn hợp Na, Ba vào nước dư thu được 900ml dung dịch A và 0,996 lít H2 (đktc). Tính Ph của dung dịch A đó?
Lời giải
NH2 = 0,996/22,4 = 0,04 mol
Gọi số mol của Na và Ba lần lượt là x và y mol.
Ta có: 23x + 137y = 4,66 (1)
Na + H2O → NaOH + ½ H2
X → x→ x/2 mol
Ba + 2H2O → Ba(OH)2 + H2
Y →y → y mol
=> x/2 + y = 0,04 (2)
Từ (1) và (2) ta có: x = 0,04 và y = 0,02
Phương trình điện ly: NaOH → Na+ + OH–
0,04 0,04 mol
Ba(OH)2 → Ba2+ + 2OH–
0,02 0,04 mol
Tổng số mol OH– là: nOH- = 0,08 mol
CM(OH-) = 0,08/0,8 = 0,1M => pOH = 1 => pH = 13
Với bài viết trên, hy vọng Top Nổi Bật đã giúp bạn giải đáp được câu hỏi về PH là gì? Công thức nồng độ Ph. Nếu như bạn vẫn còn điều gì thắc mắc hãy nhanh tay comment ngay ở bài viết bên dưới để chúng tôi giúp bạn giải đáp thắc mắc đó nhanh nhất nhé.







